5)脱盐:蛋白质、酶用盐析法沉淀分离后,常需脱盐才能获得纯品。最常用的脱盐方法是透析法,如图2-1所示:把蛋白质溶液装入透析袋中,袋的二端用线扎紧,然后用蒸馏水或缓冲液进行透析,这时盐离子通过透析袋扩散到水或缓冲液中,蛋白质分子量大不能穿透析袋而保留在袋内,通过不断更换蒸馏水或缓冲液,直至袋内盐分透析完毕。透析需要较长时间,常在低温下进行,并加入防腐剂避免蛋白质和酶的变性或微生物的污染。
此外用葡聚糖凝胶脱盐的效果也很好,其原理和应用方法在这里不赘述。
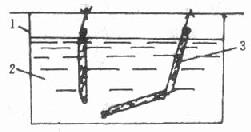
图2-1 透析装置图
(2)有机溶剂沉淀法:有机溶剂能降低溶液的电解常数,从而增加蛋白质分子上不同电荷的引力,导致溶解度的降低;另外,有机溶剂与水的作用,能破坏蛋白质的水化膜,故蛋白质在一定浓度的有机溶剂中的溶解度差异而分离的方法,称“有机溶剂分段沉淀法”,它常用于蛋白质或酶的提纯。使用的有机溶剂多为乙醇和丙酮。高浓度有机溶剂易引起蛋白质变性失活,操作必须在低温下进行,并在加入有机溶剂时注意搅拌均匀以避免局部浓度过大。由此法析出的沉淀一般比盐析容易过滤或离心沉降,分离后的蛋白质沉淀,应立即用水或缓冲液溶解,以降低有机溶剂浓度。操作时的pH值大多数控制在待沉淀蛋白质的等电点附近,有机溶剂在中性盐存在时能增加蛋白质的溶解度,减少变性,提高分离的效果,在有机溶剂中添加中性盐的浓度为0.05mol/L左右,中性盐过多不仅耗费有机溶剂,可能导致沉淀不好。沉淀的条件一经确定,就必须严格控制,才能得到可重复的结果。有机溶剂浓度通常以有机溶剂和水容积比或用百分浓度表示。有机溶剂沉淀蛋白质分辨力比盐析法好,溶剂易除去;缺点是易使酶和具有活性的蛋白质变性。故操作时要求条件比盐析严格。对于某些敏感的酶和蛋白质,使用有机溶剂沉淀尤其要小心。
(3)等电点沉淀法:利用蛋白质在等电点时溶解度最低而各种蛋白质又具有不同等电点的特别进行分离的方法,称为等电点沉淀法。但在等电点时,各种蛋白质仍有一定的溶解度而使沉淀不完全,同时许多蛋白质的等电点十分接近,故单独使用此法效果不理想,分辨力也差。大多用于提取后去除杂蛋白,即利用变动提取液的pH值使某些与待提纯的蛋白质等电点相距较大的杂蛋白从溶液中沉淀出。实际工作中常把等电点沉淀和盐析法、有机溶剂沉淀法联合使用。
(4)吸附法:在蛋白质的提纯方法中,选择性吸附也是应用历史较久迄今仍在广泛采用的方法之一。早期工作常用高岭土 (我国的一种土质,其分子式大致是AL2O3·2SiO2·2H2O)、氧化铝(AL2O3)及活性炭等吸附剂,由于这些吸附剂吸附力较弱,或者易引起蛋白质变性而应用不广,现已为凝胶性吸附剂所代替,如氢氧化铝凝胶和磷酸钙凝胶,尤其后者使用最广。吸附剂的应用有两种不同方式。当蛋白质较易吸附时,可以选择适当条件主要吸附蛋白质而分离去杂质;当蛋白质较难吸附时,则选择利于吸附杂质条件将杂质与蛋白质分开。有时两种方法可先后使用,以达到较高的提纯目的。吸附条件通常在微酸性条件(pH5~6)及稀盐溶液中进行,盐浓度过高会干扰对蛋白质及酶的吸附,亦即是说需要用更多量的吸附剂才能达到一定结果。洗脱时一般在弱碱条件下或适当提高洗脱液离子强度,可将吸附的蛋白质或酶完全洗脱下来。
吸附操作可以用静态吸附,也可以用柱层析吸附,即将凝胶装成柱进行吸附操作。凝胶装柱后如溶液的通过能力很差,可用助滤剂(如硅藻土)和凝胶混合,当调整二者的比例时得到一系列通过能力和吸附能力不同的层析柱。最近还使羟基磷灰石[Ca10(PO4)6.(OH)2]分离蛋白质和酶,它可以在高盐浓度下吸附中性及酸性蛋白质而排除碱性蛋白质。吸附常在pH6.8的磷酸缓冲液中进行。洗脱完全时凝胶可反复使用3~4次,吸附杂质较多的凝胶以0.1mol/L氢氧化钠或1mol/L盐酸洗净后再用。医学.全在.线www.med126.com
(5)离子交换法:蛋白质和酶都具有电解质性质,故可用离子交换剂进行分离提纯,特别是经过了初步纯化后的蛋白质和酶采用此法效果尤为显著。有关离子交换剂及其使用技术,参阅有关专著,这里介绍近年来以纤维素衍生物作为离子交换剂纯化蛋白质及酶的方法。在这类衍生物中以二乙氨基乙基纤维素(简称DEAE-纤维素,为阴离子交换剂)及甲基纤维素(简称CM-纤维素,为阳离子交换剂)应用最广泛。
DEAE-纤维素是纤维素结构中的氢原子被一定量的二乙氨基-乙基取代而成弱碱性化合物,它作为阴离子交换剂的原理是:

在实际工作中常用磷酸缓冲液平衡DEAE-纤维素后,才对蛋白质进行交换吸附的,故上式B-可视为PO3-。用DEAE-纤维素吸附酶和蛋白质时常用pH为7~9,然后提高盐浓度(使蛋白质与交换剂的结合键减弱)或降低pH使之洗脱,洗脱后的蛋白质溶液有时可进一步上CM-纤维素柱纯化。作为阳离子交换剂,CM-纤维素吸附蛋白质的原理如下:

式中A+可为H+或Na+,视平衡CM-纤维素时所用溶剂而定。CM-纤维素常选在pH4.5~6.0左右吸附蛋白质,然后提高pH或盐浓度进行洗脱。离子交换纤维素对大分子物质有较大交换量,例如CM-纤维素对血红蛋白的交换量为93~98mg/100mgCM-纤维素。此外,纤维素离子交换剂还具有层析条件温和、物质易于洗脱、分辨力强、被分离的蛋白质不易变性等优点。
除了纤维素离子交换剂外,离子交换凝胶也是目前应用于分离蛋白质和酶的一种很好的离子交换剂。常用的有DEAE-葡聚糖凝胶和CM-葡聚糖凝胶。离子交换凝胶不仅具有交换当量高、层析条件温和、操作简便等优点,而且兼具分子筛的性能,在梯度洗脱时,对不同分子量的蛋白质具有很高的分辨能力。
2.核酸的分离纯化 从细胞中提取核酸后,仍混杂着蛋白质、多糖和各种大小分子核酸同类物。除去这些“杂质”的过程,也就是核酸提纯过程。在核酸的分离纯化时,为防止核酸大分子的变性降解,必须在0~4℃的低温条件下操作。核酸酶的水解作用,是过去制备具有活性核酸大分子的严重障碍,现普遍采用加入去污剂或加入EDTA、8-羟基喹啉、柠檬酸钠以除去核酸酶的激活剂Mg2+,就可以抑制核酸酶的活性,保证在提纯过程中核酸大分子的完整。关于核酸分离纯化阶段中除去多糖、蛋白质及不同类型核酸之间分离的一些方法,分别介绍如下:
(1)肝糖元、淀粉及粘多糖,由于其物理化学性质与核酸有许多相似之处,常在提取液中残存下来。除去的方法常有:①取材前尽量减少组织中多糖的含量,如先使动物饥饿数天然后杀死,可使细胞内肝糖元大大减少。②加入淀粉酶,将大分子多糖分解为小分子,在以后纯化步骤中逐渐被除去。③在浓磷酸盐存在下,以2-甲氧基乙醇抽提核酸提取液,使多糖溶于下层水相,核酸在上面有机层中。④以钙盐沉淀DNA,再以草酸钾处理,使之形成DNA钾盐回收,然后用离子交换法吸附DNA,使之与多糖分离。
(2)蛋白质的除去:由于核酸在细胞内以核蛋白体形式存在,不论采用哪种方法提取核酸,蛋白质都不同程度地存在于体系中。因此,除去蛋白质是核酸分离纯化不可避免的步骤。常用方法有下列几种:①加入去污剂如硫酸十二脂钠,从提取到分离纯化各阶段均可反复使用此法。去污剂与氯仿法或苯酚法结合使用,效果更加理想。②氯仿-戊醇或辛醇对提取液摇荡抽提,蛋白质在氯仿-水界面形成凝胶,离心后除去,核酸留在水溶液中。此法在分离纯化中也常反复使用。③苯酚水溶液抽提,在对氨基水杨酸等阴离子化合物存在下,DNA或RNA都可以进入水相,蛋白质则沉淀于酚层,然后取水相加入乙醇或2-乙氧基乙醇沉淀RNA或DNA,残余的酚可用葡聚糖凝胶G-10或G-25除去。
 |
 |
 |
2019医学职称考试题库 免费试用>> |
|
| 85514人已试用 客服咨询:13588130315 |
||