11、水蒸气通过灼热的C(石墨)发生下列反应:
H2O(g) + C(s) = CO(g) + H2(g)
此平衡系统的组分数K=( ),自由度数f=( )。
① 1 ② 2 ③ 3 ④ 4
12、某中草药含有效药物成分B,它与水形成互不相溶体系,现采用水蒸汽蒸馏分离出B,已知此体系在98℃沸腾,此温度下,Po(H2O)=9.426104Pa,PBo =3.466103Pa,MB=128,现欲蒸出1kg的B,需消耗水蒸汽( )kg。
① 0.26 ② 0.011 ③ 193.39 ④ 3.82
13、25℃时,相同浓度(均为0.01mol.kg--1)的La(NO3)3,Mg(NO3)2和NaNO3三种电解质水溶液,离子平均活度系数由小到大的顺序是( )。
① La(NO3)3 > Mg(NO3)2 > NaNO3
② La(NO3)3 > NaNO3 > Mg(NO3)2
③ Mg(NO3)2 > La(NO3)3 > NaNO3
④ NaNO3 > Mg(NO3)2 > La(NO3)3
14、H2SO4的水溶液,其离子平均活度与离子平均活度系数及其质量摩尔浓度m的关系是( )。
① =271/4 •(m/ mo ) ② =•(m/ mo )
③ = 41/3 •(m/ mo ) ④ =43 •(m/ mo)3
15、在25℃时电池反应H2(g)+½O2(g)=H2O(l)所对应的标准电池电动势为E1o,则反应2H2O(l)=2H2(g)+O2(g)所对应的电池的标准电动势E2o为( )。
① E2o= -2E1o ② E2o= 2E1o
③ E2o = - E1o ④ E2o =E1o
三、填空题(20分)
1、 ( )过程的所有状态函数的变化值都等于零,而封闭体系( )过程和孤立体系中可逆过程△S都等于零。
2、在一定温度下的抽空容器中,NH4HCO3(s)进行如下分解反应:
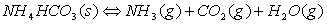
达到平衡时所产生的气体总压力为P,则此反应的标准平衡常数Kθ与T的关系式为( )。
3、对反应 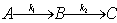 , 用稳态近似法处理的重要条件是
, 用稳态近似法处理的重要条件是
k1( )k2 。(填写数学符号)。
4、反应 2A→G为双分子反应,A消耗1/3的时间和消耗2/3的时间相差9秒,A消耗1/3的时间为( )秒。
5、反应 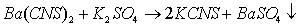 ,在Ba(CNS)2过量的情况下,生成BaSO4溶胶,胶团的结构式为( )。
,在Ba(CNS)2过量的情况下,生成BaSO4溶胶,胶团的结构式为( )。
6、表面活性剂物质由( )组成,在达到( )浓度时,溶液的某些物理性质发生转折。
7、对物质B来说,在正常沸点时,气相的化学势B(g)( )液相的化学势B(l);此时将压力P(=101.325kPa)保持不变,而升高温度,则气相的化学势B(g)( )液相的化学势B(l)。 [填写“等于”、“大于”或“小于” ]
8、盐AB可形成以下几种水合物:
AB•H2O(s), 2AB•5H2O(s) ,2AB•7H2O(s)和 AB•6H2O(s),所有这些水合物都有相合的熔点。这个盐水体系有( )个低共熔点。
9、当电流密度增大时,原电池的端电压( ),电解池的分解电压( ) 。[填写“增大”或“减小” 或“不变”]
10、在10cm3 1mol.dm-3KOH中加入10cm3水,其摩尔电导率将( ) 。 [填写“增加”、“减少”或“不变”]
四、简答题(20分)
1、某理想气体在300K下,从状态I变到状态II时,Q=1000 J,
 ,判断该过程是否可逆,为什么?
,判断该过程是否可逆,为什么?
2、化学动力学和化学热力学所解决的问题有何不同? 举例说明。
3、试根据热力学原理推断气体在固体表面的吸附过程一定放热。
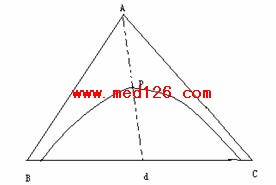
4、在101325Pa,25℃时,醋酸(A)-氯仿(B)-水(C)三组分相图如下(图中P点为临界点)
(1) 指出101325Pa,25℃时,B与C组成的体系属于括号内哪一类双液体系(完全互溶,完全不互溶,部分互溶)
(2) 在组成为的d的B-C混合液中,不断加入A时,体系将发生什么变化?
5、下列电极构成浓差电池,从理论上判断哪一个是正极?哪一个负极?
Ag | AgCl(s) Cl-(1M); Ag | AgCl (s) Cl-(110-2M)