| 通用名 | 复方磺胺嘧啶片 |
| 曾用名 | |
| 英文名 | COMPOUND SULFADIAZINE TABLETS |
| 拼音名 | FUFANG HUANG'AN MIDING PIAN |
| 药品类别 | 磺胺类 |
| 性状 | 本品为白色片。 |
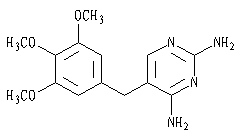
| 药理毒理 | 品为磺胺嘧啶(SD)与甲氧苄啶(TMP)的复方制剂,
两者合用具有协同抗菌作用,对非产酶金黄色葡萄球菌、化
脓性链球菌、肺炎链球菌、大肠埃希菌、克雷伯菌属、沙门
菌属、变形杆菌属、摩根菌属、志贺菌属等肠杆菌科细菌、
淋病奈瑟菌、脑膜炎奈瑟菌、流感嗜血杆菌均具有良好抗菌
活性。此外在体外对沙眼衣原体、星形奴卡菌、疟原虫和弓
形虫也有抗微生物活性。近年来细菌对本品的耐药性普遍存
在,尤其如志贺菌属等肠道菌科的细菌,故目前临床上很少
使用。
本品作用机制为磺胺药作用于二氢叶酸合成酶,干扰合
成叶酸的第一步,而甲氧苄啶作用于叶酸合成代谢的第二
步,选择性抑制二氢叶酸还原酶的作用,因此二者合用,可
使细菌的叶酸代谢受到双重阻断,具有协同抗菌作用,较单
药的耐药菌株减少, |
| 药代动力学 | 本品中的磺胺嘧啶和甲氧苄啶口服后自胃肠道吸收完
全,均可吸收给药量的90%以上,吸收后二者均可广泛分布
于全身组织和体液中。并穿透血脑屏障至脑脊液中,达治疗
浓度,也可穿过血胎盘屏障,进入胎儿血循环。30%~40%的
磺胺嘧啶以及80%~90%的甲氧苄啶以原型自尿中排出。磺胺
嘧啶的消除半衰期为8~13小时,甲氧苄啶的消除半衰期为
8~10小时。 |
| 适应症 | 近年来由于许多临床常见病原菌对本品耐药,故治疗细
菌感染需参考药敏试验结果,复方磺胺嘧啶的主要适应症为
敏感菌株所致的下列感染:
1.大肠埃希杆菌、克雷伯菌属、肠杆菌属、奇异变形杆
菌、普通变形杆菌和莫根菌属敏感菌株所致的尿路感染。
2.肺炎链球菌或流感嗜血杆菌所致的急性中耳炎。
3.肺炎链球菌或流感嗜血杆菌所致的成人慢性支气管
炎急性发作。 |
| 用法用量 | 成人常用量 口服,一次2片,一日2次。
小儿常用量 2个月以上体重40kg以下的婴幼儿按体
重口服SD 20~30mg/kg及TMP 4~6mg/kg,每12小时1次;
体重40kg以上的儿童剂量同成人常用量。 |
| 不良反应 | 1.过敏反应较为常见,可表现为药疹,严重者可发生渗
出性多形红斑、剥脱性皮炎和大疱表皮松解萎缩性皮炎等;
也有表现为光敏反应、药物热、关节及肌肉疼痛、发热等血
清病样反应。
2.中性粒细胞减少或缺乏症、血小板减少症,偶可发生
再生障碍性贫血。患者可表现为咽痛、发热和出血倾向。
3.溶血性贫血及血红蛋白尿。这在缺乏葡萄糖-6-磷酸
脱氢酶的患者应用磺胺药后易于发生,在新生儿和小儿中较
成人为多见。
4.高胆红素血症和新生儿核黄疸。由于磺胺药与胆红素
竞争蛋白结合部位,可致游离胆红素增高。新生儿肝功能不
完善,故较易发生高胆红素血症和新生儿黄疸,偶可发生核
黄疸。
5.肝脏损害。可发生黄疸、肝功能减退,严重者可发生
急性肝坏死。
6.肾脏损害。可发生结晶尿、血尿和管型尿。偶有患者
发生间质性肾炎或肾小管坏死的严重不良反应。
7.恶心、呕吐、胃纳减退、腹泻、头痛、乏力等,一般
症状轻微,不影响继续用药。偶有患者发生艰难梭菌肠炎,
此时需停药。
8.甲状腺肿大及功能减退偶有发生。
9.中枢神经系统毒性反应偶可发生,表现为精神错乱、
定向力障碍、幻觉、欣快感或抑郁感。一旦出现均需立即停
药。
10.偶可发生无菌性脑膜炎、有头痛、颈项强直、恶心
等。
磺胺药所致的严重不良反应虽少见,但可致命,如渗出
性多形红斑、剥脱性皮炎、大疱表皮松解萎缩性皮炎、暴发
性肝坏死、粒细胞缺乏症、再生障碍性贫血等血液系统异常。
治疗时应严密观察,当皮疹或其他反应早期征兆出现时即应
立即停药。 |
| 禁忌症 | 1.对磺胺类药物和甲氧苄啶过敏者禁用;
2.孕妇、哺乳期妇女禁用;
3. 2个月以下婴儿、早产儿禁用;
4.肝肾功能不良者、血液病患者(如白细胞减少、血小
板减少、紫癜症等)禁用。 |
| 注意事项 | 1.下列情况应慎用:缺乏葡萄糖-6-磷酸脱氢酶、血卟
啉症、叶酸缺乏性巨幼红细胞性贫血或其他血液系统疾病、
失水、休克和老年患者。
2.交叉过敏反应。对一种磺胺药呈现过敏的患者对其他
磺胺药亦可能过敏。
3.对呋塞米、砜类、噻嗪类利尿药、磺脲类、碳酸酐抑
制药呈现过敏的患者,对磺胺药亦可过敏。
4.每次服用本品时应饮用足量水分。服用期间也应保持
充足进水量,使成人尿量每日至少维持在1200ml以上。如
应用本品疗程长,剂量大时除多饮水外宜同服碳酸氢钠。
5.治疗中须注意:
(1)定期周围血象检查,疗程长、服用剂量大、老年、
营养不良及服用抗癫痫药者易出现叶酸缺乏症,如周围血象
中白细胞或血小板等已有明显减少则需停用本品。
(2)应定期尿液检查(每2~3日查尿常规一次)以发现
长疗程或高剂量治疗时可能发生的结晶尿。
(3)肝、肾功能检查。
6.严重感染者应测定血药浓度,对大多数感染疾患者游
离磺胺浓度达50~150μg/ml(严重感染120~150μg/ml)
可有效。总磺胺血浓度不应超过200μg/ml,如超过此浓度,
不良反应发生率增高。
7.不可任意加大剂量、增加用药次数或延长疗程,以防
蓄积中毒。
8.由于本品能抑制大肠杆菌的生长,妨碍B族维生素在
肠内的合成,故使用本品超过一周以上者,应同时给予维生
素B以预防其缺乏。
9.如因服用本品引起叶酸缺乏时,可同时服用叶酸制
剂,后者并不干扰TMP的抗菌活性,因细菌并不能利用已合
成的叶酸。如有骨髓抑制征象发生,应即停用本品,并给予
叶酸3~6mg肌注,一日1次,使用3日或根据需要用药至
造血功能恢复正常,对长期、过量使用本品者可给予高剂量
叶酸并延长疗程。
10.下列情况不宜应用本品:
(1)中耳炎的预防或长程治疗。
(2)A组溶血性链球菌刻扁桃体炎和咽炎,因不易清除细
菌。 |
| 孕妇及哺乳期妇女用药 | 1.磺胺嘧啶和TMP都可穿过血胎盘屏障至胎儿体内,动
物实验发现均有致畸作用。人类研究缺乏充足资料,孕妇宜
避免应用。
2.磺胺嘧啶可自乳汁中分泌,乳汁中浓度约可达母体
血药浓度的50%~100%,药物可能对婴儿产生影响,特别
是葡萄糖-6-磷酸脱氢酶缺乏的新生儿导致溶血性贫血的可
能。TMP也可分泌至乳汁中,其浓度较高,且药物有可能干
扰哺乳婴儿的叶酸代谢。鉴于上述原因,哺乳期妇女暂停应
用本品。 |
| 儿童用药 | 由于磺胺药可与胆红素竞争在血浆蛋白上的结合部位,
而新生儿的乙酰转移酶系统未发育完善,磺胺游离血浓度增
高,以致增加了核黄疸发生的危险性,因此该类药物在新生
儿及2个月以下婴儿属禁忌。 |
| 老年患者用药 | 老年患者应用磺胺药时发生严重不良反应的机会增加,
如严重皮疹、骨髓抑制和血小板减少等。应用TMP易出现叶
酸缺乏症。因此老年患者宜避免应用,确有指征时需权衡利
弊后决定。 |
| 药物相互作用 | 1.与尿碱化药合用可增加磺胺药在碱性尿中的溶解度,
使排泄增多。
2.对氨基苯甲酸可代替磺胺被细菌摄取,对磺胺药的抑
菌作用发生拮抗,因而两者不宜合用。也不宜与含对氨苯甲
酰基的局麻药如普鲁卡因、苯佐卡因、丁卡因等合用。
3.与口服抗凝药、口服降血糖药、甲氨蝶呤、苯妥英钠
和硫喷妥钠合用时,上述药物需调整剂量,因本品中的磺胺
嘧啶可取代这些药物的蛋白结合部位,或抑制其代谢,以致
药物作用时间延长或发生毒性反应。因此当这些药物与本品
同时应用,或在应用本品后使用均需调整其剂量。
4.骨髓抑制药与本品合用时可能增强此类药物对造血
系统的不良反应,如白细胞、血小板减少,应严密观察可能
发生的毒性反应。
5.与避孕药(口服含雌激素者)长时间合用可导致避孕
的可靠性减小,并增加经期外出血的机会。
6.与溶栓药物合用时,可能增大其潜在的毒性作用。
7.与肝毒性药物合用,可能引起肝毒性发生率的增高。
对此类患者尤其是用药时间较长及以往有肝病史者应监测
肝功能。
8.与光敏药物合用可能发生光敏作用相加。
9.接受磺胺药治疗者对维生素K的需要量增加。
10.乌洛托品在酸性尿中可分解产生甲醛,后者可与磺
胺形成不溶性沉淀物,使发生结晶尿的危险性增加,因此两
药不宜同时应用。
11.磺胺药可取代保泰松的血浆蛋白结合部位,当两者
合用时可增强保泰松的作用。
12.因本品有可能干扰青霉素类药物的杀菌作用,最好
避免与此类药物同时应用。
13.与磺吡酮合用时可减少本品中的磺胺嘧啶自肾小管
的分泌,其血药浓度升高而持久,易产生毒性反应,因此在
应用磺吡酮期间或应用其治疗后可能需要调整本品的剂量。
14.TMP可抑制华法林的代谢而增强其抗凝作用。
15.TMP与环孢素合用可增加肾毒性。
16.利福平与本品合用可明显使TMP清除增加和血清半
衰期缩短。
17.TMP不宜与抗肿瘤药、2,4-二氨基嘧啶类药物同
时应用,也不宜在应用其他叶酸拮抗药治疗的疗程之间应用
本品,因为有产生骨髓再生不良或巨幼红细胞贫血的可能。
18.与氨苯砜合用会致氨苯砜和TMP两者血药浓度均升
高,氨苯砜浓度的升高使不良反应增多且加重,尤其是高铁
血红蛋白血症的发生。
19.与普鲁卡因胺合用时本品中的TMP可减少普鲁卡因
胺肾清除,致普鲁卡因胺及其代谢物NAPA的血浓度增高。 |
| 药物过量 | 过量服用本品会出现恶心、呕吐、头晕、头痛、嗜睡、
神智不清、骨髓抑制等。逾量的处理方法:
(1)洗胃。
(2)同时给尿液酸化药促进本品排泄。
(3)支持疗法。
(4)血液透析。
长期服用本品会引起骨髓抑制,造成血小板、白细胞的
减少和巨幼红细胞性贫血。当出现骨髓抑制症状时,患者应
立即停药同时每天肌内注射甲酰四氢叶酸5~15mg,直至造
血功能恢复正常。 |
| 贮藏 | 遮光 ,密封保存。 |
| 包装 | |
| 有效期 | |